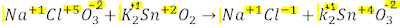La materia viva e inerte se puede encontrar en diversos estados de agrupación diferentes. Esta agrupación u organización puede definirse en una escala de organización que sigue de la siguiente manera de menor a mayor organización.
Subatómico:
Este nivel es el más simple de todo y está formado por electrones, protones y neutrones, que son las distintas partículas que configuran el átomo.
Átomo:
Es el siguiente nivel de organización. Es un átomo de oxígeno, de hierro, de cualquier elemento químico.
Moléculas:
Las moléculas consisten en la unión de diversos átomos diferentes para formar, por ejemplo, oxígeno en estado gaseoso (O2), dióxido de carbono, o simplemente carbohidratos, proteínas, lípidos...
Célula:
Las moléculas se agrupan en unidades celulares con vida propia y capacidad de autor replicación.
Tejido:
Las células se organizan en tejidos: epitelial, adiposo, nervioso, muscular...
Órganos:
Los tejidos están estructuras en órganos: corazón, bazo, pulmones, cerebro, riñones...
Aparato o Sistema:
Los órganos se estructuran en aparatos digestivos, respiratorios, circulatorios, nerviosos...
Individuo:
Nivel de organización superior en el cual las células, tejidos, órganos y aparatos de funcionamiento forman una organización superior como seres vivos: animales, plantas, insectos,...
Población:
Los organismos de la misma especie se agrupan en determinado número para formar un núcleo poblacional: una manada de leones, o lobos, un bosque de arces, pinos...
Comunidad:
Es el conjunto de seres vivos de un lugar, por ejemplo, un conjunto de poblaciones de seres vivos diferentes. Está formada por distintas especies.
Ecosistema:
Es la interacción de la comunidad biológica con el medio físico, con una distribución espacial amplia.
Biosfera:
Es todo el conjunto de seres vivos y componentes inertes que comprenden el planeta tierra, o de igual modo es la capa de la atmósfera en la que existe vida y que se sustenta sobre la litosfera.
Sistema Solar:
Se denomina Sistema Solar a nuestro sistema planetario, conformado por el Sol, en torno al cual giran nueve planetas, con sus respectivos satélites naturales (el satélite natural de la Tierra es conocido con el nombre de Luna) y diversos asteroides (trozos de roca).
Vía Láctea:
La Vía Láctea es aquella galaxia en la cual se encuentran el sistema solar y el planeta tierra, su aspecto es el de una franja ancha de luz blanca y difusa que atraviesa de forma oblicua la mayor parte de la esfera celeste y cuando se la mira a través de un telescopio se descubre que está compuesta por infinidad de estrellas, aproximadamente, el cálculo dice que son entre 200 y 400 millones las estrellas.
Cada nivel de organización engloba a los niveles inferiores anteriores. Por ejemplo, un elefante tiene un sistema respiratorio que consta de órganos como son los pulmones, que a su vez están compuestos de tejidos como el tejido respiratorio, el epitelial, que a su vez lo conforman células, y así sucesivamente.
El universo es enorme… lleno de misterios…

Fuente:http://www.cienciaybiologia.com/bgeneral/niveles-organizacion.htm
 >DESCOMPOSICION:
>DESCOMPOSICION: 
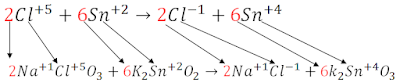
 >DOBLE DESPLAZAMIENTO O SUSTITUCIÓN:
>DOBLE DESPLAZAMIENTO O SUSTITUCIÓN: